Cyanure de triméthylsilyle
| Cyanure de triméthylsilyle | |||
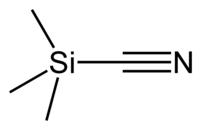
| |||
 | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | triméthylsilylformonitrile | ||
| Synonymes |
cyanotriméthylsilane |
||
| No CAS | |||
| No ECHA | 100.028.780 | ||
| No CE | 231-657-3 | ||
| SMILES | |||
| InChI | |||
| Apparence | liquide | ||
| Propriétés chimiques | |||
| Formule | C4H9NSi [Isomères] |
||
| Masse molaire[1] | 99,206 5 ± 0,004 3 g/mol C 48,43 %, H 9,14 %, N 14,12 %, Si 28,31 %, |
||
| Propriétés physiques | |||
| T° fusion | 8-11 °C[2] | ||
| T° ébullition | 114-117 °C[2] | ||
| Masse volumique | 0,793 g·cm-3[2] | ||
| Point d’éclair | 1 °C[2] | ||
| Propriétés optiques | |||
| Indice de réfraction | 1,392[2] | ||
| Précautions | |||
| Directive 67/548/EEC | |||
| Transport | |||
|
|||
| Unités du SI et CNTP, sauf indication contraire. | |||
| modifier |
|||
Le cyanure de triméthylsilyle est le composé organique de formule semi-développée (CH3)3SiCN. Ce liquide volatil consiste en un groupe cyanure, -CN lié à un groupe triméthylsilyle.
Cette molécule est utilisée en synthèse organique comme équivalent à l'acide cyanhydrique (HCN). Elle est préparée par réaction du cyanure de lithium et du chlorure de triméthylsilyle[3]:
- LiCN + (CH3)3SiCl → (CH3)3SiCN + LiCl
Dans sa principale application, le cyanure de triméthylsilyle s'additionne sur une double liaison carbone-oxygène comme sur les aldéhydes:
- RCHO +(CH3)3SiCN → RCH(CN)OSi(CH3)3
Le produit est une cyanohydrine O-silylée.
Un autre usage de ce réactif est la conversion de pyridine-N-oxydes en 2-cyanopyridines. Cette réaction est plus efficace dans le dichlorométhane en utilisant du chlorure de diméthyl carbomyl comme électrophile activant. Il est aussi possible d'utiliser du chlorure de benzoyle mais le rendement et la régiosélectivité de l'addition du groupe cyano est moins bonne.
Enfin par réaction avec C6F5XeF, il fournit le composé organoxénon C6F5XeCN[4].
Sécurité[modifier | modifier le code]
Le cyanure de triméthylsilyle doit être manipulé avec beaucoup de précautions car il s'hydrolyse facilement en donnant de l'acide cyanhydrique:
- 2 (CH3)3SiCN + H2O → (CH3)3SiOSi(CH3)3 + 2 HCN
Notes[modifier | modifier le code]
- (en) Cet article est partiellement ou en totalité issu de l’article de Wikipédia en anglais intitulé « Trimethylsilyl cyanide » (voir la liste des auteurs).
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- Cyanure de triméthylsilyle sur sigmaaldrich.com
- Livinghouse, T., Trimethylsilyl Cyanide: Cyanosilation of p-Benzoquinone, Org. Synth., coll. « vol. 7 », , p. 517
- H. Frohn, C6F5XeF, a versatile starting material in xenon-carbon chemistry, Journal of Fluorine Chemistry, 2004, vol. 125(6), p. 981–988. DOI 10.1016/j.jfluchem.2004.01.019.




