Fluorure de sélénoyle
| Fluorure de sélénoyle | |
| |
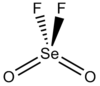
| Structure du fluorure de sélénoyle | |
| Identification | |
|---|---|
| No CAS | |
| PubChem | 23236013 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | F2O2Se |
| Masse molaire[1] | 148,96 ± 0,03 g/mol F 25,51 %, O 21,48 %, Se 53,01 %, |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le fluorure de sélénoyle, ou oxyfluorure de sélénium, est un composé chimique de formule SeO2F2. Il se présente sous forme gazeuse aux conditions normales de température et de pression. La molécule présente une géométrie tétraédrique distordue avec un angle O=Se=O de 126,2°, un angle O=Se–F de 108,0° et un angle F–Se–F de 94,1°[2]. La liaison Se–F a une longueur de 168,5 pm tandis que la liaison Se=O a une longueur de 157,5 pm[3].
Le fluorure de sélénoyle peut être obtenu par réaction d'acide fluorosulfurique HFSO3 chauffé sur le séléniate de baryum BaSeO4 ou l'acide sélénique H2SeO4. La réaction du trioxyde de sélénium (en) SeO3 avec le tétrafluorure de sélénium SeF4 peut produire du fluorure de sélénoyle parmi d'autres oxyfluorures de sélénium.
Le fluorure de sélénoyle est plus réactif que le fluorure de sulfuryle SO2F2. Il s'hydrolyse et se réduit plus facilement que ce dernier. Il peut réagir violemment au contact de l'ammoniac NH3.
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Wai-Kee Li, Gong-du Zhou et Thomas C. W. Mak, Advanced structural inorganic chemistry, 2008, p. 651. (ISBN 0-19-921694-0)
- (en) Kolbjørn Hagen, Virginia R. Cross et Kenneth Hedberg, « The molecular structure of selenonyl fluoride, SeO2F2, and sulfuryl fluoride, SO2F2, as determined by gas-phase electron diffraction », Journal of Molecular Structure, vol. 44, no 2, , p. 187-193 (DOI 10.1016/0022-2860(78)87027-6, Bibcode 1978JMoSt..44..187H, lire en ligne)
