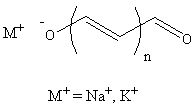Polyméthine
Les polyméthines constituent une classe de colorants possédant le motif —(CH=CH—)n.
Structure[modifier | modifier le code]
Les polyméthines comportent un nombre impair de groupements CH reliés au sein d'une chaîne carbonée conjuguée en zigzag. Suivant les groupes d'atomes à l'extrémité de la chaîne, le colorant polyméthine se décline en différentes familles[1].
Streptopolyméthines-cyanées[modifier | modifier le code]
Le préfixe strepto (=tordu) rappelle que la chaîne est en zigzag.
Les polyméthines cyanées, également appelées cyanines, contiennent un atome d'azote à chaque extrémité de la chaine polyméthine, un des atomes d'azote étant chargé positivement. Il constitue donc un centre électro-attracteur alors que l'autre N est un centre électrodonneur. Il en résulte un effet donneur accepteur (push-pull, littéralement pousse-tire). Les autres familles de polyméthines (voir ci-dessous) peuvent être comparées à cette famille.
Les groupes d'atomes qui diffèrent d'une polyméthine à l'autre influent sur la charge électrique portée par le colorant, et donc sur nombre de ses propriétés. La polyméthine cyanée est cationique, et donc associée à un contre-anion.
Streptopolyméthine-oxonol[modifier | modifier le code]
La polyméthine-oxonol est chargé négativement. Un contre-cation est donc présent avec l'oxonol.
Les oxonols peuvent être à la base de polyméthines à chaîne plus longues comme dans la synthèse suivante[2], basée sur une double condensation de Knoevenagel. Le contre-ion est dans ce cas Na+.

Streptopolyméthine-mérocyanine[modifier | modifier le code]
La polyméthine mérocyanée n'est pas chargée, mais les groupes d'atomes placés de part et d'autre de la chaîne conjuguée possèdent des effets électroniques qui polarisent la molécule. Le groupe carbonyle est attracteur à un bout de la chaîne polyméthine alors que le groupe amine, à l'autre extrémité, est donneur. L'effet push-pull est donc toujours présent.
Squaraine[modifier | modifier le code]
La polyméthine squaraine est un zwitterion, portant un groupe chargé positivement et un autre chargé négativement. Les squaraines n'ont donc pas de contre-ion.
Autres polyméthines[modifier | modifier le code]
Les colorants possédant le squelette triphénylméthane peuvent être considérés comme des polyméthines pontées. Cela introduit un caractère aromatique aux propriétés de la polyméthine, ce qui complique les règles de prévision des couleurs[3],[4].
Des groupements barbituriques ou thiobarbituriques ont été décrits de part et d'autre du motif principal —(CH=CH—)n[5]. Ces colorants ont notamment montré leur intérêt dans le suivi cinétique de certaines réactions enzymatiques, notamment celle de pectines lyases et polygalacturonases[6].
Propriétés et usage[modifier | modifier le code]
Les colorants polyméthines cyanées ont régné sur le monde de la photographie et des autres applications des colorants depuis 1856[7].
De nos jours, ces composés sont considérés comme la principale source de composés organiques fluorescents dans le domaine des grandes longueurs d'onde et pouvant être excités dans la plage 600 - 900 nm.
Les squaraines sont une des seules familles de colorants utilisables comme sonde fluorescente dans le proche infrarouge. Leur bande d'absorption est fine et intense, dans le visible ou le proche infrarouge. Leur photoconductivité est grande et leurs caractéristiques photophysiques appropriées pour la détection fluorescente sélective de biomolécules telles que les protéines dans des applications biologiques ou biomédicales[8].
Notes et références[modifier | modifier le code]
- Amaresh Mishra, Rajani K. Behera, Pradipta K. Behera, Bijaya K. Mishra, & Gopa B. Behera (2000), Cyanines during the 1990s: A Review, Chem. Rev. 100, 1973-2011.
- Org. Lett vol. 10, No. 19, 2008.
- Dähne, S. Science 1978, 199, 1163.
- Zbigniew R. Grabowski & Krystyna Rotkiewicz (2003), Structural Changes Accompanying Intramolecular Electron Transfer: Focus on Twisted Intramolecular Charge-Transfer States and Structures, Chem Rev, 103, 3899-4031.
- (en) Arthur Desvals, Mariagrazia Fortino, Corentin Lefebvre et Johann Rogier, « Synthesis and characterization of polymethine dyes carrying thiobarbituric and a carboxylic acid moieties », New Journal of Chemistry, (ISSN 1369-9261, DOI 10.1039/D2NJ00684G, lire en ligne, consulté le )
- Mustapha Nedjma, Norbert Hoffmann et Abdel Belarbi, « Selective and Sensitive Detection of Pectin Lyase Activity Using a Colorimetric Test: Application to the Screening of Microorganisms Possessing Pectin Lyase Activity », Analytical Biochemistry, vol. 291, no 2, , p. 290–296 (ISSN 0003-2697, DOI 10.1006/abio.2001.5032, lire en ligne, consulté le )
- Williams, C. H. G. Trans. R. Soc. Edinburg 1856, 21, 377.
- M. Sameiro T. Gonçalves (2009). Fluorescent Labeling of Biomolecules with Organic Probes, Chem. rev. 109, 190–212.