Réactif de Lawesson
| Réactif de Lawesson | |

| |
| Identification | |
|---|---|
| Nom UICPA | 2,4-disulfure de 2,4-bis(4-méthoxyphényl)-1,3-dithia-2,4-diphosphétane |
| No CAS | |
| No ECHA | 100.038.944 |
| No CE | 242-855-4 |
| PubChem | 87949 |
| SMILES | |
| InChI | |
| Propriétés chimiques | |
| Formule | C14H14O2P2S4 [Isomères] |
| Masse molaire[1] | 404,467 ± 0,033 g/mol C 41,57 %, H 3,49 %, O 7,91 %, P 15,32 %, S 31,71 %, |
| Propriétés physiques | |
| T° fusion | 229 °C [2] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
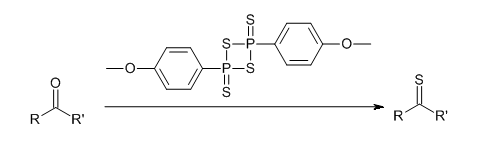
Le réactif de Lawesson est un composé chimique organique utilisé comme agent de thionation[3]. Il a été rendu populaire par Sven-Olov Lawesson qui n'est toutefois pas son inventeur[réf. souhaitée].
Le réactif de Lawesson est plus réactif que le réactif de Belleau, mais moins que les réactifs de Davy.
Thionation[modifier | modifier le code]
La réaction de thionation convertit un carbonyle en thiocarbonyle. Le réactif de Lawesson est le réactif le plus utilisé, car il permet de travailler à des températures plus élevées que le sulfure d'hydrogène et est plus soluble dans les solvants organiques que le pentasulfure de diphosphore.
Mécanisme[modifier | modifier le code]
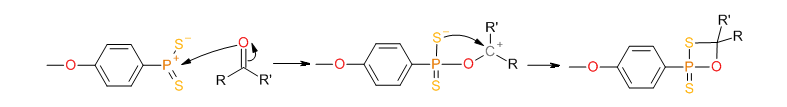
Les sites actifs de la molécule sont activés par l'ouverture du cycle central formé par les phosphores et les soufres. Cette ouverture se fait principalement par voie thermique:
Les ylures de dithiophosphines aussi mis à jour peuvent réagir avec le groupe carboxyle pour former un intermédiaire thiaoxaphosphétane:
La formation d'une double liaison stable P=O déplace la réaction vers la droite et conduit à la séparation de l'intermédiaire:
Cette réaction ressemble à la réaction de Wittig et est valable pour les cétones, les amides et les lactames. Les esters réagissant dans des conditions réactionnelles plus agressives, il est possible d'effectuer des thionations sélectives[4].
Production et synthèse[modifier | modifier le code]
Le réactif de Lawesson est synthétisé à partir d'anisole et de pentasulfure de diphosphore[5].

Voir aussi[modifier | modifier le code]
Notes et références[modifier | modifier le code]
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) « Réactif de Lawesson », sur ChemIDplus, consulté le 18 janvier 2010
- (en) M. T. Molina, M. Yanez, O. Mo, R. Notario et J.-L. M. Abboud, The thiocarbonyl groupe, Chichester/New York/Brisbane etc., John Wiley & Sons Ltd, coll. « The functional group chemistry / The chemistry of double-bonded functional group », , 1858 p. (ISBN 0-471-95956-1)
- (en) Martin Jesberger, Thomas P. Davis et Leonie Barner, « Applications of Lawesson's Reagent in Organic and Organometallic Syntheses », Synthesis, vol. 13,
- Thomsen, I.; Clausen, K.; Scheibye, S.; Lawesson, S.-O., Thiation with 2,4-Bis(4-methoxyphenyl)-1,3,2,4-Dithiadiphosphetane 2,4-disulfide: N-Methylthiopyrrolidone, Org. Synth., coll. « vol. 7 », , p. 372